[A12158114]申請書類の書き方に関するFDAガイドライン:臨床と統計
(税込) 送料込み
商品の説明
商品説明
【30日間返品保証】: 商品説明に誤りがある場合は、無条件で弊社送料負担で商品到着後30日間返品を承ります。
ご満足のいく取引となるよう精一杯対応させていただきます。
下記に商品説明や配送料・配送方法・注意事項等の説明がございます。お客様にとって大切な事柄を記載しておりますので、よくお読みいただき、ご了解の上ご購入をお願い致します。
【インボイス制度対応済み】当社では2023年10月からインボイス制度に対応した適格請求書発行事業者番号(通称:T番号・登録番号)を印字した納品書(明細書)を商品に同梱してお送りしております。こちらをご利用いただくことで、税務申告時や確定申告時に消費税額控除を受けることが可能になります。こちらの商品は、とヤフーショッピングの併売商品です。どちらのサイトからもご購入可能です。
●本店はこちら
●2号店はこちら
●ヤフーショッピング本店はこちら
●ヤフーショッピング2号店はこちら【・ヤフーショッピングセール情報】
セール商品はこちら
ヤフーショッピングセール商品はこちら【商品説明】
商品詳細
■商品名■
申請書類の書き方に関するFDAガイドライン:臨床と統計
■出版社■
ライフサイエンス出版
■著者■
日本製薬工業協会 医薬品評価委員会 臨床評価部会 臨床試験における統計学的諸問題検討分科会
■発行年■
1991/08/01
■ISBN10■
4897750598
■ISBN13■
9784897750590
■コンディションランク■
良い
コンディションランク説明
ほぼ新品:未使用に近い状態の商品
非常に良い:傷や汚れが少なくきれいな状態の商品
良い:多少の傷や汚れがあるが、概ね良好な状態の商品(中古品として並の状態の商品)
可:傷や汚れが目立つものの、使用には問題ない状態の商品
■コンディション詳細■
箱付き。書き込みありません。古本のため多少の使用感やスレ・キズ・傷みなどあることもございますが全体的に概ね良好な状態です。水濡れ防止梱包の上、迅速丁寧に発送させていただきます。参考書・予備校テキストの買取もしています↓ 【その他の注意事項】
お取引に関わるその他の注意事項 【書き込みに関して】
書き込みの程度や付属品の揃い具合はできるだけチェックはしておりますが、多少(10%~20%程度)の誤差や見落としがあることもございます。恐れ入りますが予めご了解いただきますようお願い申し上げます。【使用感などの状態に関して】
商品説明のコンディションランクをご参照ください。【画像および商品説明に関して】
出品している商品および付属物などは画像はサンプル画像となります。書籍の状態につていはご質問いただいてもご回答が出来かねる場合がございます。【落札後のキャンセルや返品に関して】
でのご落札後のキャンセルは承っておりません。責任を持って取引できる価格でのご入札をお願いいたします。
商品説明と著しく異なる点があった場合や異なる商品が届いた場合は、到着後30日間は無条件で着払いでご返品後に返金させていただきます。メール又は取引メッセージにてご連絡ください。商品に瑕疵がない状態での落札者様都合でのご返品は承っておりません。
12939円[A12158114]申請書類の書き方に関するFDAガイドライン:臨床と統計本、雑誌健康と医学平成25年度 医療機器開発ガイドライン策定事業 事業報告書"https://m.media-amazon.com/images/I/81D6dsTS72L._AC_UF1000,1000_QL80_.jpg","https://sathuki-blog.medicomazawa.co.jp/wp-content/uploads/2022/11/image-1.png","https://sathuki-blog.medicomazawa.co.jp/wp-content/uploads/2023/05/image-18.png","https://sathuki-blog.medicomazawa.co.jp/wp-content/uploads/2022/12/image-39.png","https://lookaside.fbsbx.com/lookaside/crawler/media/?media_id=790184623108943"申請書類の書き方に関するFDAガイドライン:臨床と統計 | 日本製薬工業
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
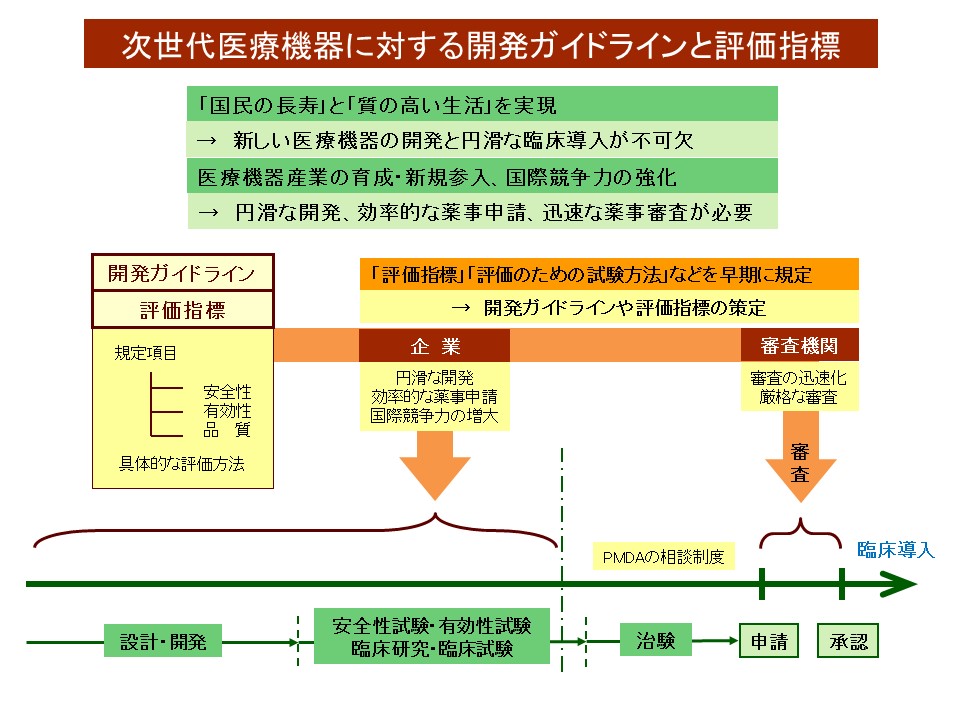
平成25年度 医療機器開発ガイドライン策定事業 事業報告書
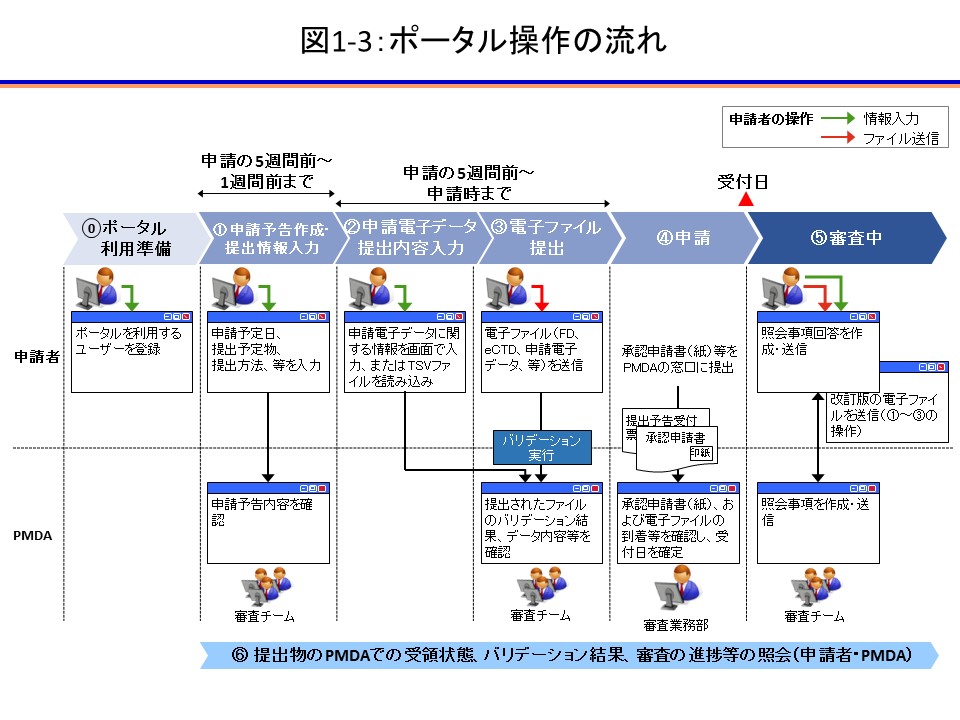
申請電子データに関する FAQ | 独立行政法人 医薬品医療機器総合機構
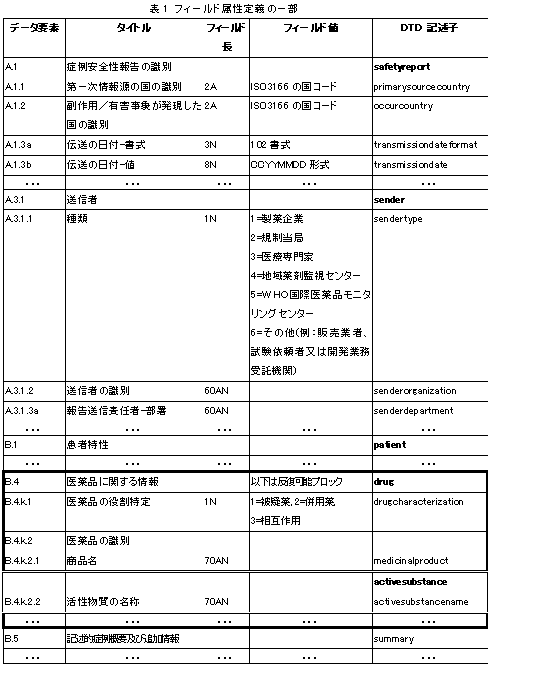
個別症例安全性報告の電子的伝送に関する概要 | 独立行政法人 医薬品
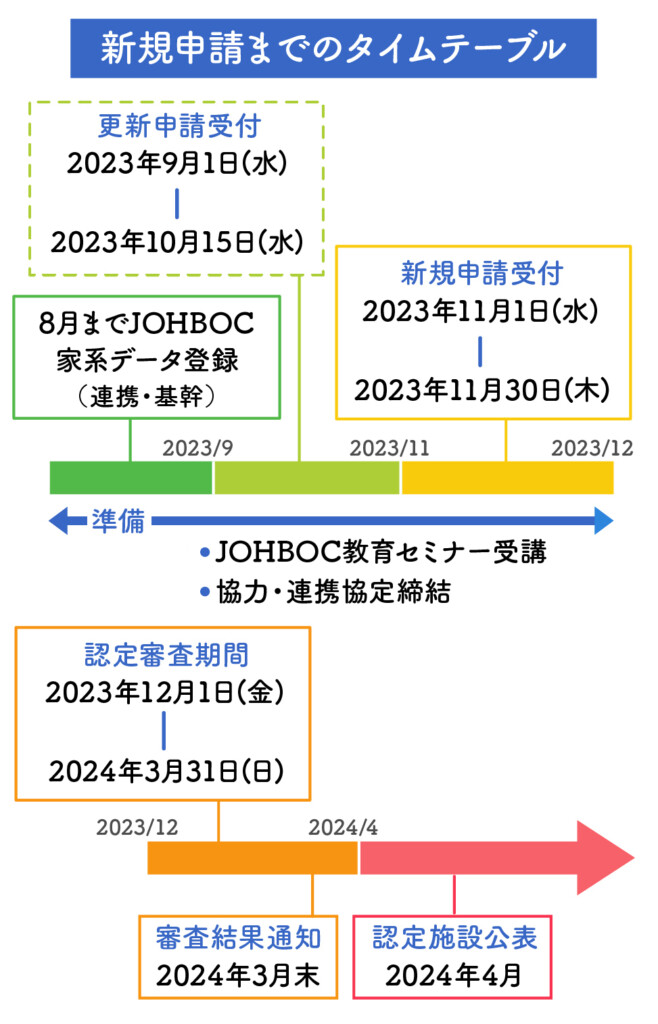
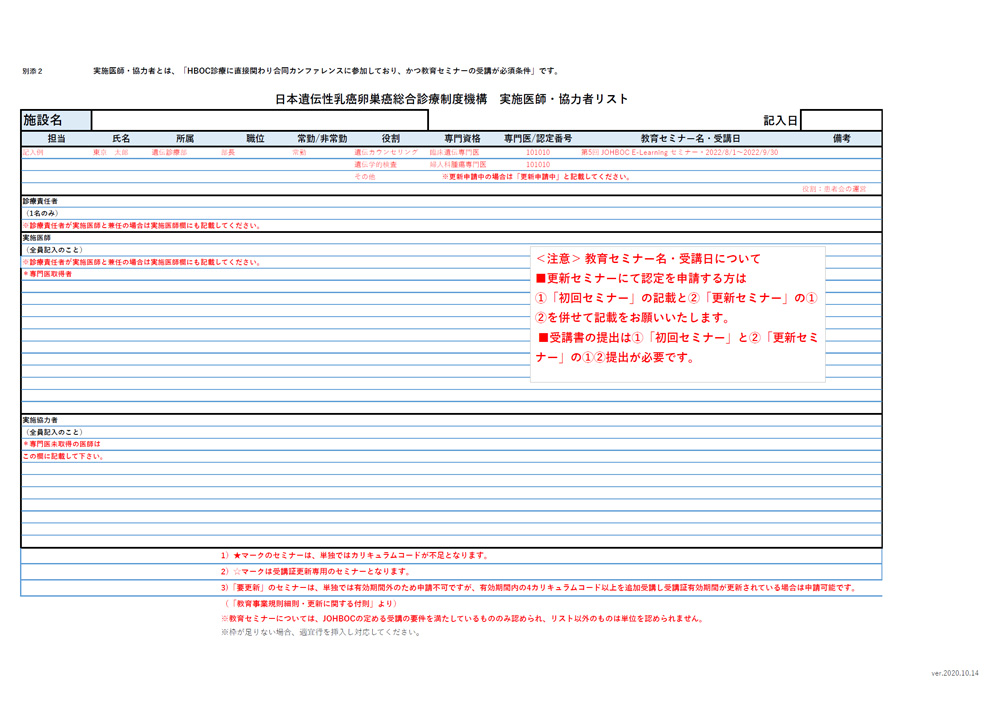
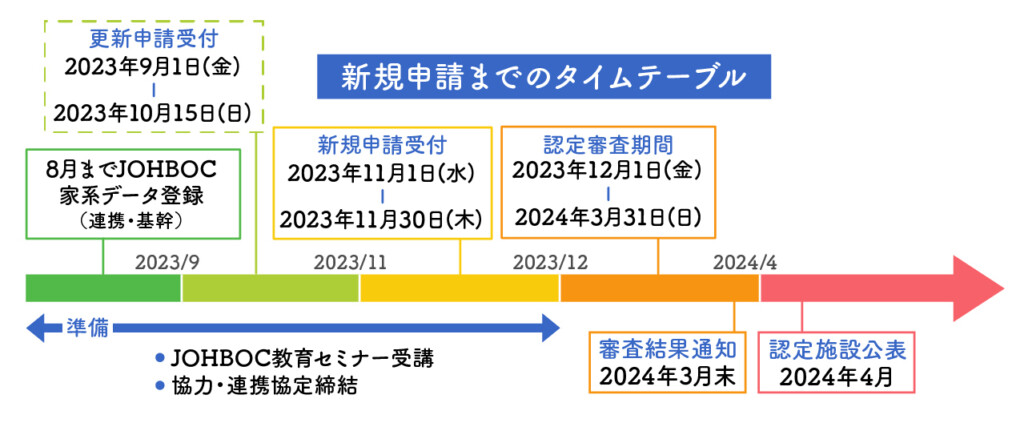
申請書類の記入例 - JOHBOCJOHBOC
医療機器の「臨床試験の試験成績に関する資料」の提出が必要な範囲等に
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
Unaltd
医療機器の薬事申請関連サービス | 株式会社コーブリッジ
Unaltd
平成 3 0年度) 主 催 厚生労働省医薬・生活衛生局 独立行政法人医薬品
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
Unaltd
Unaltd
申請書類の記入例 - JOHBOCJOHBOC
認証申請の手続き|医療機器の認証|公益財団法人 医療機器センター
プロジェクトOrbis】レンビマ+キイトルーダの併用療法、3カ国同時承認
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
海外における医薬品・医療機器 審査制度、審査実態等調査及び分析業務
Unaltd
申請FDA-醫療器材
定番の中古商品 大腸内視鏡検査ハンドブック/丹羽寛文(著者) 臨床医学
申請手続きと提出資料 - 認定臨床研究審査委員会
経典ブランド [A12228041]耳下腺腫瘍臨床の最前線Q&A 臨床医学
輪之内町がん患者医療用補正具購入費助成事業実施要綱
データの提供 - NBDCグループ共有データベース
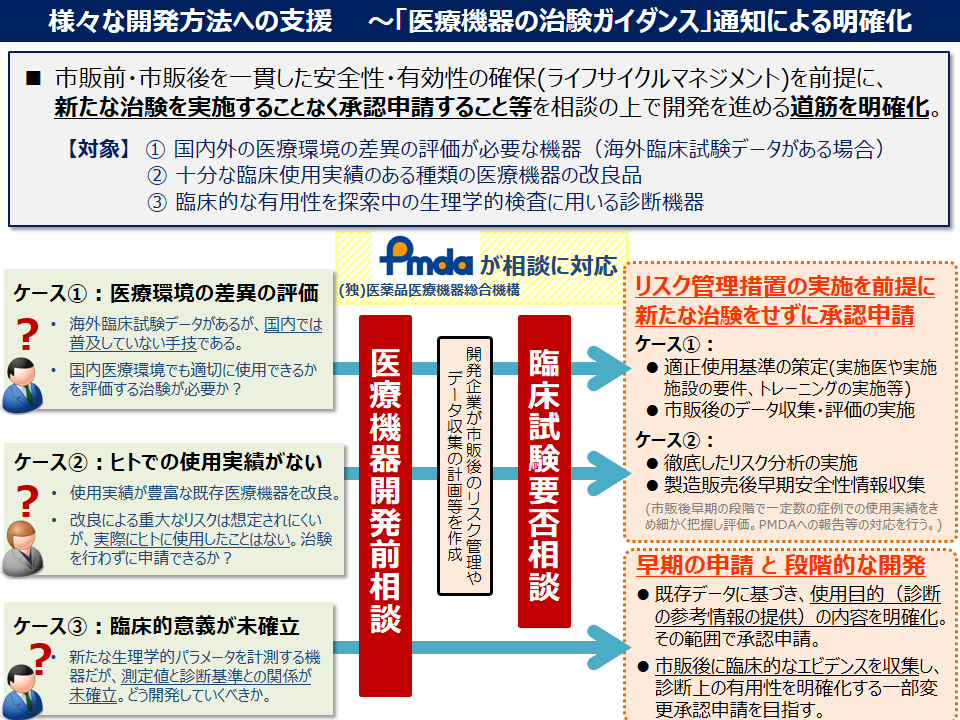
最適使用推進ガイドラインのねらい | 株式会社メディカルエデュケ-ション
4.2.1. 新規登録 — 経費旅費 / 管理者操作ガイド 第25版 2023-11-01
申請書類の書き方に関するFDAガイドライン:臨床と統計 | 日本製薬工業
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
申請書類の書き方に関するFDAガイドライン:臨床と統計-
平成25年度 医療機器開発ガイドライン策定事業 事業報告書
申請電子データに関する FAQ | 独立行政法人 医薬品医療機器総合機構
個別症例安全性報告の電子的伝送に関する概要 | 独立行政法人 医薬品
申請書類の記入例 - JOHBOCJOHBOC
医療機器の「臨床試験の試験成績に関する資料」の提出が必要な範囲等に
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
Unaltd
医療機器の薬事申請関連サービス | 株式会社コーブリッジ
Unaltd
平成 3 0年度) 主 催 厚生労働省医薬・生活衛生局 独立行政法人医薬品
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
Unaltd
Unaltd
申請書類の記入例 - JOHBOCJOHBOC
認証申請の手続き|医療機器の認証|公益財団法人 医療機器センター
プロジェクトOrbis】レンビマ+キイトルーダの併用療法、3カ国同時承認
申請書類の記入例 - JOHBOCJOHBOC
申請書類の記入例 - JOHBOCJOHBOC
海外における医薬品・医療機器 審査制度、審査実態等調査及び分析業務
Unaltd
申請FDA-醫療器材
定番の中古商品 大腸内視鏡検査ハンドブック/丹羽寛文(著者) 臨床医学
申請手続きと提出資料 - 認定臨床研究審査委員会
経典ブランド [A12228041]耳下腺腫瘍臨床の最前線Q&A 臨床医学
輪之内町がん患者医療用補正具購入費助成事業実施要綱
データの提供 - NBDCグループ共有データベース
最適使用推進ガイドラインのねらい | 株式会社メディカルエデュケ-ション
4.2.1. 新規登録 — 経費旅費 / 管理者操作ガイド 第25版 2023-11-01
商品の情報
メルカリ安心への取り組み
お金は事務局に支払われ、評価後に振り込まれます
出品者
スピード発送
この出品者は平均24時間以内に発送しています







.jpg)
.jpg)










![経典ブランド [A12228041]耳下腺腫瘍臨床の最前線Q&A 臨床医学](https://auctions.c.yimg.jp/images.auctions.yahoo.co.jp/image/dr000/auc0410/users/d4fab30473777a8019148ae00533fa27693af6d4/i-img345x500-1697730495ulagqu748275.jpg)